细胞外囊泡的类型:从外泌体到癌小体和介于两者之间的一切
在细胞外囊泡(EV)研究人员的某些圈子中,“外泌体(exosome)”一词已经成为一个非常容易混淆的词。造成这种现象的原因是多方面的,但最主要的原因是命名法,以及仅根据其大小来定义囊泡的缺陷。然而,尽管国际细胞外囊泡学会(International Society of Extracellular Vesicles, ISEV) [1] 做出了极大的努力,但这个词在文献中一直很流行,尽管在ISEV相关的出版物中没有。研究人员使用“外泌体”这个术语可能是因为它太容易识别了,或者可能是因为他们已经习惯了它。其他人可能在讨论小细胞外囊泡时使用“外泌体”,而没有意识到在他们的分离物中可能有非外泌体的细胞外囊泡。这就引出了一个问题,外泌体到底是什么,它与其他EV有什么不同?
外泌体和其他细胞外囊泡亚型-它们形成的方式
细胞外囊泡EV是指任何(细胞外)的囊泡,其具有双层膜,包含随机的或者可特定反映某种细胞状态的细胞内容物,并由细胞“自然”产生(即不是通过挤压细胞人为产生)。这一定义包括多种细胞外囊泡亚型,其中许多可能尚未发现或确定特征。在此,EV领域的一个主要限制是:EV的特性是混杂的。亚型在大小、组成和密度上重叠,使它们几乎无法区分。它们的生物起源确实不同(图1),这是定义它们的唯一因素。不幸的是,除非这条起源路线被目击,否则几乎不可能为一种EV指定一条生源路线。外泌体必须被看到其生成过程才能被相信。
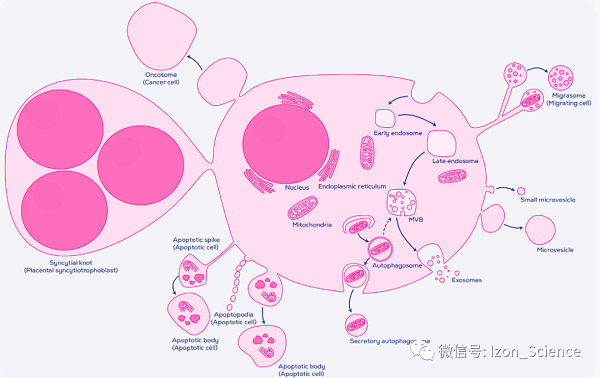
图1所示。细胞外囊泡(EV)生物发生的不完全示意图。从顶部开始,膜内陷形成胞内体(endosome),这是一个细胞内的间隔,可以走向不同的命运之一。在这里,我们展示了向晚期胞内体的转变,晚期胞内体可以成熟为多泡体(MVB),腔内囊泡内陷到MVB中。然后MVBs与质膜融合,释放这些腔内囊泡,这些囊泡现在被称为外泌体 (exosome)。我们还可以看到迁移细胞在长而薄的膜突起上留下的迁移体(migrasome)。迁移体的球形肿胀可能脱落或恶化释放其腔内囊泡。接下来是微囊泡 (microvesicles),体积既可小(大小与外泌体重叠),也可大,它们直接从质膜上产生。至于分泌性自噬小体 (secretory autophagosome),在这里,一个双层包裹的自噬小体与质膜融合,释放出一个单层的分泌性自噬小体,可能包含整个细胞器。接下来我们来看看细胞凋亡的产物。凋亡小体 (Apoptotic bodies) 既直接从膜泡形成,也直接从凋亡或微管棘突形成。当凋亡细胞撤退时,也会留下珠状的凋亡伪足。目前描述的最大的EV是合胞节,它是直接从胎盘的合胞滋养层表面发芽的细胞核集合。最后一种是癌小体 (oncosome),像凋亡小体或微泡一样直接从细胞膜上出芽,但具体来源于癌细胞,通常体积更大。
那么,这些难以捉摸的外泌体(exosome)到底是什么?外泌体是直径约为30 ~ 150 nm大小的小EV。外泌体的直径可小至30 nm,而10 ~ 20 nm是脂质双层囊泡的最小大小,因此这也是EV大小的下限 [2]。也就是说,如果你要测量比它小的东西,它就不是EV。外泌体是由晚期胞内体内陷形成腔内囊泡(ILV)并使晚期胞内体形成多泡体(MVB)而产生的。然后MVB与质膜融合,释放外泌体(之前以腔内囊泡的形式存在)到细胞外空间,如图1所示。
另一方面,微囊泡(microvesicles)直接从质膜向外发芽,并且往往体积更大。微囊泡又被称为核外颗粒体或微粒,其大小与外泌体重叠,并一直延伸到直径超过一微米。
当质膜出芽的EVs在细胞凋亡的背景下发生时,这些被称为凋亡小体(apoptotic bodies)。这些凋亡的EVs可能甚至比微囊泡更大,但可能载有独特的货物,包括完整(或碎片)的细胞器和大量碎片化的遗传物质。
许多其他亚型一般也在细胞中常见,也存在于特定情况下(见图1)。例如,包括神经元释放的突触囊泡,或胎盘释放的脱落合胞节(shed syncytial knot),后者从胎盘释放,从多核合胞滋养细胞中去除细胞核团 (图1左侧) [3]。图1中显示的许多EV类型未得到充分研究,而且所有EV(包括外泌体和微囊泡)都知之甚少。事实上,似乎我们对这些有趣的囊泡研究得越多,就越意识到我们对它们了解甚少。在过去的几年里,有一种无知的自信让我们相信我们可以区分外泌体和微囊泡。但最近,这一点似乎越来越不确定。
EV亚型的真正特异性标志物可能不存在
本节的标题可能有点难以置信,但它是有文献支持的。虽然曾经认为某些细胞成分是针对不同EV亚型的,但对EV生物发生和释放的细胞生物学研究使这一观点受到质疑。然而,外泌体的真正标志物在某种程度上是该领域的圣杯,因为人们(无论正确与否)痴迷于研究EV的外泌体成分。在使用尺寸排阻分离富含小EV上清液前,他们通过超速离心沉淀较大EV,然后0.22µm过滤。具有讽刺意味的是,许多名为“外泌体提取”的商业试剂盒并不是专门针对这种亚型的。然而,这个名字在该领域几乎令人上瘾。怎么知道EV是外泌体呢? 初步的答案是你可能不能。
转运所需的胞内体分选复合物(ESCRT)蛋白曾被认为对外泌体具有特异性。线索就在它们的名字里,人们认为它们是胞内体,所以只能存在于外泌体中。不幸的是,事实证明并非如此。ESCRT I、II和III蛋白复合物及相关蛋白(甚至长期以来被认为是外泌体标志物的TSG101)参与了微囊泡从质膜出芽以及ILV出芽到MVB [4-6]。
ESCRT-0复合体可能(这里强调为“可能”)具有胞内体特异性,使其组分成为外泌体的潜在标志物。有证据表明,基因敲除降低两种ESCRT-0蛋白的表达减少了CD63+ve的小EV的释放。因此,CD63是外泌体来源的,对么?
这可能是错误错的。CD9、CD81和CD63等四跨膜蛋白长期以来一直被吹捧为外泌体标志物,但它们也存在于微泡上 [6]。具体而言,Mathieu等人(2021)的一项研究发现,CD63和CD9均阳性的EVs至少部分是质膜出芽(因此是微囊泡),而CD63+ve CD9-ve 的EVs最有可能是外泌体。再次强调是“可能”。
那么syntenin-1呢?由于其参与了ESCRT相关蛋白Alix的募集,因此被建议作为外泌体标志物。它也存在于CD63+ve和CD9+ve的EV中,但至少在CD63+ve 的EV中富集 [6]。因此,虽然syntenin-1可能在外泌体中富集,但它可能不足以作为外泌体的标记物。
当然,经常被用作外泌体标记的Alix本身经得起推敲么?不幸的是没有。研究发现Alix在CD63+ve和CD9+ve EVs中存在的可能性相同 [6],这表明Alix可能不具有外泌体特异性。
Mathieu等人(2021)将LAMP1和/或LAMP2确定为潜在的外泌体标志物 [6]。LAMPs是溶酶体的标记物,在CD63+ve EVs中的表达显著高于CD9+ve EVs。可信的外泌体标记物?也许……
再次值得强调的是,已经使用的外泌体标志物可能被确定为非特异性。但Mathieu等人(2021)的研究仅使用了一种细胞类型,即有争议的HeLa细胞,因此结果尚不能完全推广到不同的细胞类型。在不同的细胞类型中重复这些发现会使它们更可信。
外泌体抑制剂和刺激剂——有用的工具还是误入歧途?
GW4869是中性鞘磷脂酶抑制剂,可抑制神经酰胺依赖的ILVs向MVBs出芽 [10]。至少在理论上是这样。这使得GW4869在许多研究中被用作“外泌体抑制剂”。实际上,这一机制可能根本不是外泌体特有的。Mathieu等人(2021)的研究表明,常用的“外泌体抑制剂”GW4869对CD63+ve CD9-ve类似外泌体的分泌几乎没有影响,作者建议谨慎使用。
相反,“外泌体刺激剂”巴佛洛霉素A1通过抑制空泡ATP酶来抑制晚期胞内体的酸化。据报道,这可能会增加外泌体的分泌 [6]。然而,虽然这在某些情况下可能有用,但重要的是要承认,改变晚期胞内体的pH可能会改变外泌体的货物装载,在使用该药物操纵外泌体分泌之前,应研究这一点。
这对EV领域意味着什么?
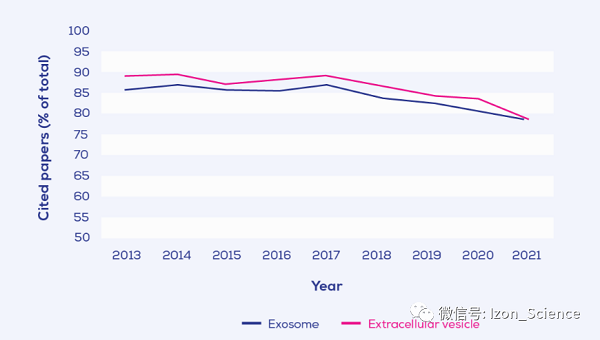
它至少意味着几件事。首先,人们在使用“外泌体”这个术语时应该更加谨慎。这是一个很棒的词,EV领域之外的人也认识它,但这并不意味着它得到了更多的引用。它不是,见图2的证据。
其次,这意味着需要更多的研究。最好使用多种细胞系,并使用多种不同的技术进行分离和鉴定。只有这样,我们才能确定外泌体标记物(无论是LAMP蛋白还是其他蛋白)是否真的是外泌体蛋白。即便如此,使用这些蛋白质进行免疫捕获也存在固有缺陷。我们不知道每个外泌体都会包含任何给定的标记。只选择那些蛋白会产生不知情偏见。

Gen 2 qEV纯化柱带给您更纯净的细胞外囊泡,如下图Gen 2 qEV10参数, 10mL人血浆上样:
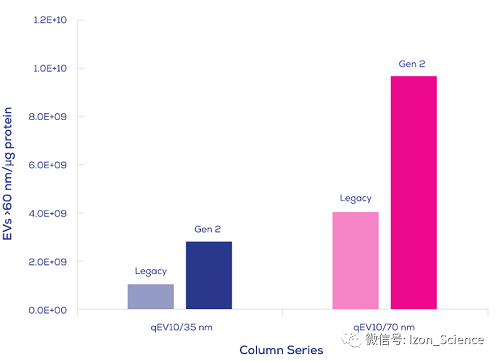
转载来源:Izon Science








 药物筛选/分子生物学
药物筛选/分子生物学