加拿大科研人员制定细胞外囊泡的不同分离技术和表征方法的入门方案

外泌体是一种直径为20 - 150nm的膜结合生物纳米囊泡,主要由内吞膜产生,并通过胞吐作用释放。它们在20世纪80年代初被首次发现,是网状细胞释放的含有转铁蛋白受体(TfR)的小膜泡,并被证明以旁分泌或内分泌方式调节生物过程,并运输各种物质,包括信使RNA (mRNA)、microRNA (miRNA)、蛋白质和脂质。正因为如此,外泌体在治疗和诊断领域引起了人们的关注,包括它们作为纳米载体将药物/分子物质运输到靶点、治疗应用和作为生物标志物。
加拿大西安大略大学的科研人员通过不同分离技术和表征细胞外囊泡的方法制定了基础的入门方案。在本研究中通过使用四种分离方法来获取细胞外囊泡,并且使用Apogee纳米流式仪对分离后的细胞外囊泡进行表征。包括:(i) 补充聚乙二醇和氯化钠条件培养基后进行低速离心;(iii)通过100 kda排除过滤器过滤条件介质;(iv)使用标准商用试剂盒进行分离。然后在分离外泌体之前,将该培养基中的细胞和碎片去除,通过0.2 mm过滤器过滤,并补充蛋白酶和RNAse抑制剂。纯化后的EVs可立即使用,或在4℃下稳定保存(长达一周用于成像或下游EVs实验),或在- 80℃下长时间保存,然后用于生化研究。本研究的目的不是比较这些方法,而是向有需要的人提供所描述方法,以便研究人员可以在各自的条件下选择 “最佳方法”分离细胞外囊泡。

富集培养基(ECM)中加入50%聚乙二醇(PEG) 8000溶液(在ddH2O中)至终浓度为10% PEG,通过倒置混合均匀,加入NaCl至终浓度为75 mM,再通过倒置混合。然后将混合物在4℃下孵育4 - 16小时。与极短的孵育时间相比,较长的孵育时间可能会增加外泌体的产量。然后将样品在16000g下在4℃下离心1小时,沉淀外泌体部分。然后将颗粒重悬在1xPBS中。为了去除颗粒中任何残留的污染物,再次重复此过程。最终的外泌体富集部分保存在1xPBS中,4℃短期保存(天),- 20℃长期保存(月),最好在- 80℃保存,但在后一种情况下,应谨慎使用低蛋白结合管。(a)PEG 8000增加了EV的沉降系数,因此可以通过低速离心分离EVs。(b)散点图的流式细胞术显示HEK293或SH-SY5Y细胞在血清耗尽(Exo -耗尽血清)或无血清的DMEM中培养基的所分泌的外泌体数量(PE标记的CD9抗体阳性EV)。
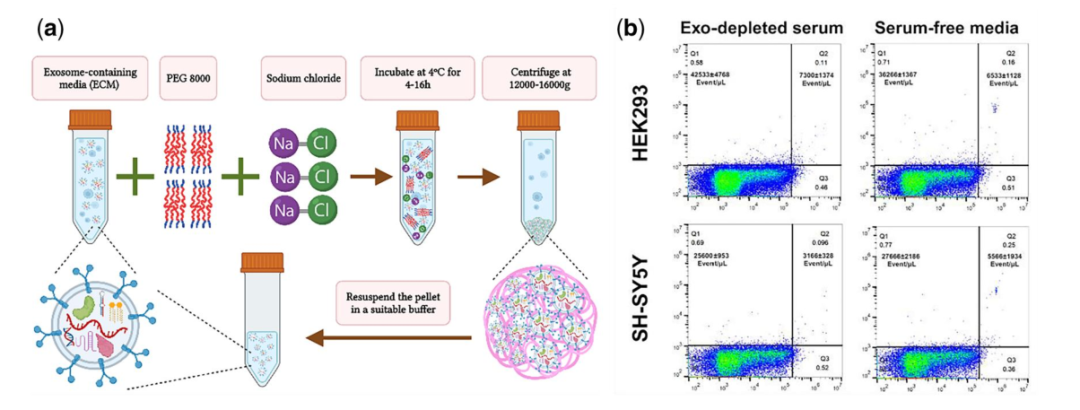
图2。基于PEG8000的EV分离。
富集培养基(ECM)在4℃下以10万g离心75-90分钟,使用适合超离心的离心管使EV聚集成沉淀。采用针穿刺技术,从管中抽出上清,在底部留下外泌体富集沉淀;将EV重悬于100 mL含蛋白酶抑制剂和RNAseOUT的冰PBS中 。(a)EV在4℃下超速离心以100,000g的75分钟,分离EVs。(b)散点图的流式细胞术显示HEK293或SH-SY5Y细胞在血清耗尽(Exo -耗尽血清)或无血清的DMEM中培养基的所分泌的外泌体数量(PE标记的CD9抗体阳性EV)。
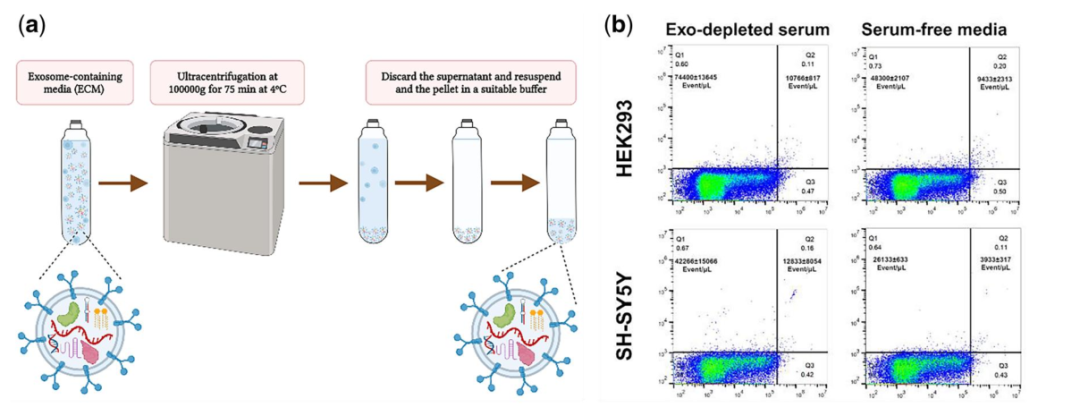
图3。基于超离心的EV的分离。
不同的过滤装置可能具有不同程度的蛋白质结合亲和力和EV的截留能力。推荐使用低蛋白结合亲和力的过滤器,如ThermoFisher PierceTM protein Concentrator PES, 100K MWCO。在这个过程中,含有外泌体富集部分会截留在过滤器上。(a)示意图。分泌组的内容物通过100 kda的过滤膜后,膜上部的上清含有外泌体富集组分。(b)散点图的流式细胞术显示HEK293或SH-SY5Y细胞在血清耗尽(Exo -耗尽血清)或无血清的DMEM中培养基的所分泌的外泌体数量(PE标记的CD9抗体阳性EV)。
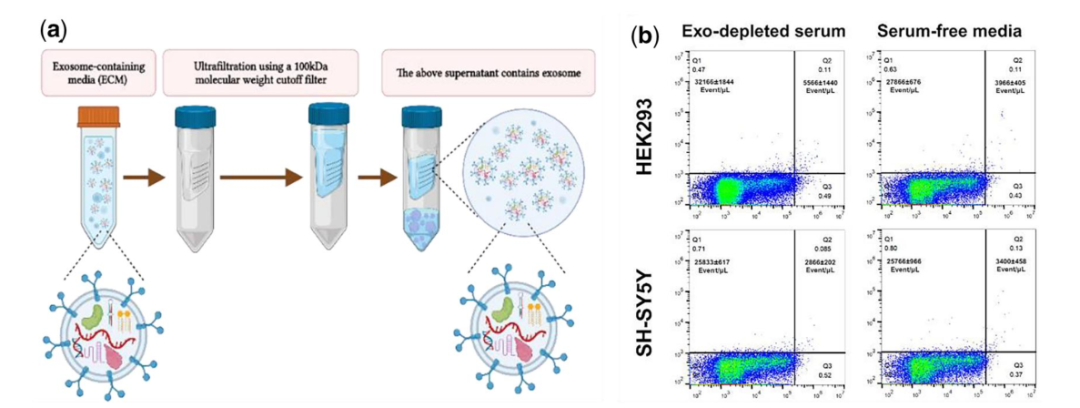
图4。基于超滤的EVs分离。
根据下游技术和所需的外泌体纯度,外泌体可以被分离出来或进一步纯化(通过超离心、蔗糖密度梯度离心或尺寸排阻)。(a)外泌体的内含物通过100 kda的过滤膜,然后通过在4℃下以100,000g离心75分钟,从膜的顶端得到的上清用于进一步纯化。(b)散点图的流式细胞术显示HEK293或SH-SY5Y细胞在血清耗尽(Exo -耗尽血清)或无血清的DMEM中培养基的所分泌的外泌体数量(PE标记的CD9抗体阳性EV)。
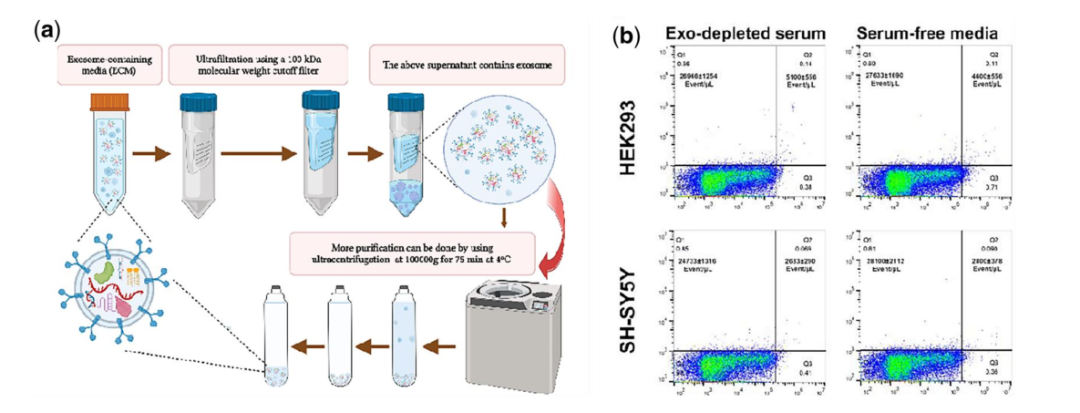
图5。基于超滤-超离心的EV分离
有几种商业试剂盒用于从不同的生物样品或细胞培养条件培养基中分离和纯化外泌体。这些试剂盒通常是基于聚合物沉淀与SEC或过滤相结合。虽然使用试剂盒可以快速提供纯外泌体,但产量可能低于“金标准”方法(如超速离心法),并且相关的成本可能使一些实验室望而却步。在这里,我们使用了一个商业套件(Exo- spinTM mini (Cell Guidance Systems LLC, USA),它同时依赖于沉淀和SEC。(a)基于Exo-spinTM迷你试剂盒的外泌体分离试剂盒示意图。外泌体溶解于试剂盒缓冲液中,离心沉淀,重悬于PBS中,然后应用于SEC进行进一步纯化。(b)散点图的流式细胞术显示HEK293或SH-SY5Y细胞在血清耗尽(Exo -耗尽血清)或无血清的DMEM中培养基的所分泌的外泌体数量(PE标记的CD9抗体阳性EV)。
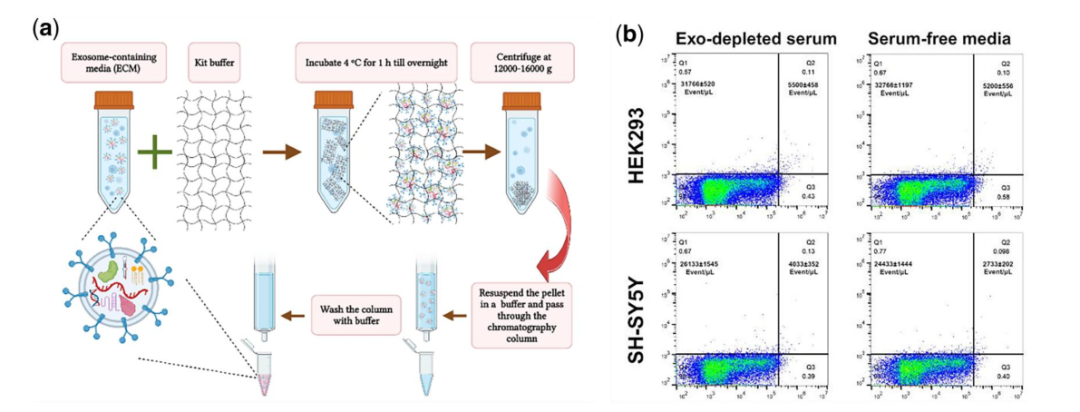
图6。基于试剂盒的外泌体提取。
结论
近年来外泌体治疗和诊断的应用呈指数增长。随着我们继续了解它们的生物发生和功能,分离和表征外泌体的试剂、技术和方案的不断发展也变得至关重要。这些进步强调了建立完善和标准化方法的必要性,并导致了增强外泌体分离和表征的协议。这些方法的不断优化已经使外泌体从复杂的生物液体(如血液、尿液和组织培养基)中纯化出来,使它们成为转化研究的宝贵资源。然而,由于不存在单一的最佳分离技术,因此每个实验室应根据研究目的、下游应用以及可用的资源/设备来选择合适的方法。
Summary

英国Apogee超灵敏纳米流式分析仪,专为外泌体微囊泡(EVs)等小颗粒分析优化设计,在EVs样品颗粒大小分析,绝对定量,多标记物同时快速分析工作中广泛应用。截止目前,该设备已累计参与数百篇高质量同行审议文章相关实验分析工作。其出色的灵敏度,稳定性及可靠性已备受业内广泛认可,并将继续为EVs相关基础研究及转化应用提供坚实支持。
Apogee纳米流式除了可用于纳米级别的颗粒 (如:细胞外囊泡、外泌体、微生物、病毒颗粒、LNP) 等,还可以用于作常规动物细胞检测 (如免疫细胞、哺乳类动物细胞、等)。它是一台全面且功能强大的纳米流式分析仪!

参考文献
OXFORD BIOLOGY Methods & Protocols,Biology Methods and Protocols,2024, bpae009
Advance Access Publication Date: 13 February 2024
Methods Article: Biomolecular, Structural and Biophysical AnalysisA methodological primer ofextracellular vesiclesisolation and characterization via different techniques
欢迎关注进科驰安官方微信(微信公众号:Bio-Gene)
回复:apogee,查看更多相关视频
长按/扫描以下二维码可识别关注公众号

广州进科驰安科技有限公司
Bio-Gene Technology Ltd.
热线:176 2009 3784
www.bio-gene.com.cn
marketing@bio-gene.com.cn
香港 北京 上海 广州 济南








 药物筛选/分子生物学
药物筛选/分子生物学